Ultimo Aggiornamento 8 Febbraio 2016
La sindrome di Hunter è una malattia genetica rara che si verifica quando un enzima necessario al corpo è assente o non funzionante.
Poiché il corpo non ha adeguate percentuali dell’enzima per abbattere alcune molecole complesse, queste possono accumularsi in quantità pericolose in alcune cellule e tessuti. L’accumulo che si verifica nella sindrome di Hunter alla fine causa un permanente danno progressivo che colpisce lo sviluppo mentale, la funzione degli organi e capacità fisiche.
La sindrome di Hunter appare in bambini di 2 anni di età, e quasi sempre si verifica nei maschi.
Non esiste cura per la sindrome di Hunter. Il trattamento della sindrome di Hunter comporta la gestione dei sintomi e delle complicazioni.
Sintomi
La sindrome di Hunter è parte di un gruppo di malattie ereditarie metaboliche chiamate mucopolisaccaridosi (MPS), la sindrome di Hunter viene indicata come MPS II. Esistono due sottotipi di sindrome di Hunter, MPS IIA e MPRS IIB. I sintomi variano a seconda del sottotipo.
Tipo MPS IIA (ad esordio precoce)
L’esordio precoce della sindrome di Hunter (MPS II) è la più comune e più grave dei due tipi e di solito compare dai 2 fino ai 4 anni. Questa forma della malattia può causare ritardo mentale grave nella tarda infanzia. I bambini con questa forma della sindrome di solito non sopravvivono oltre l’adolescenza.
Segni e sintomi di MPS II includono:
- Un calo nella capacità di sviluppo
- Mutazioni dei tratti del viso, tra cui l’ispessimento delle labbra, della lingua e delle narici
- Un naso largo e narici dilatate
- Lingua sporgente
- Irregolarità scheletriche
- ingrandimento degli organi interni, come il fegato e milza, con conseguente distensione addominale
- Difficoltà respiratorie tra cui apnea del sonno
- Disturbi cardiovascolari, quali l’ispessimento progressivo delle valvole cardiache, pressione alta (ipertensione) e ostruzione dei vasi sanguigni
- Danni alla vista
- Lesioni cutanee sul braccia e schiena
- Progressiva perdita dell’udito
- Comportamento aggressivo
- Ritardo nella crescita
- Rigidità articolare
- Diarrea
Tipo MPS IIB (esordio tardivo)
L’insorgenza tardiva della sindrome di Hunter (MPS IIB) è più mite e causa sintomi meno gravi che appaiono molto più tardi. Questa forma è di solito diagnosticata dopo i 10 anni. Sviluppo intellettuale e sociale di solito sono quasi normali. Le persone con questo tipo di sindrome di Hunter possono vivere più a lungo.
Segni e sintomi di MPS IIB sono:
- Dimensioni o forma anormale delle ossa e altre irregolarità scheletriche ( meno gravi che nella forma MPS IIA )
- Ritardo nella crescita
- Scarsa visione periferica
- Rigidità articolare
- La perdita dell’udito
Cause
La sindrome di Hunter si verifica quando un enzima che serve per abbattere gli zuccheri complessi chiamati glicosaminoglicani è mancante o non funzionante.
Nelle persone non colpite, questi enzimi sono presenti in alcune parti delle cellule del corpo conosciutw come lisosomi. I lisosomi utilizzano enzimi per abbattere i glicosaminoglicani, come parte del normale recupero del corpo e del processo di rinnovamento. In una persona con sindrome di Hunter o un’altra forma di MPS, questi enzimi o sono mancanti o non funzionano correttamente.
Normalmente, le sostanze nutritive che vengono metabolizzate da lisosomi aiutano il corpo a costruire ossa, cartilagini, tendini, cornee, pelle, tessuto connettivo, e il liquido che lubrifica le articolazioni.
Quando questo enzima non funziona correttamente, i glicosaminoglicani si raccolgono nelle cellule, sangue e tessuti connettivi, causando danni permanenti e progressivi. La sindrome di Hunter e altre forme di MPS sono a volte chiamate malattie da accumulo lisosomiale.
Nel caso di sindrome di Hunter, l’enzima mancante o non funzionante è chiamato iduronato-2-solfatasi.
La sindrome di Hunter si sviluppa quando un cromosoma difettoso viene ereditato dalla madre del bambino.
Fattori di rischio
Ci sono due principali fattori di rischio per lo sviluppo di sindrome di Hunter:
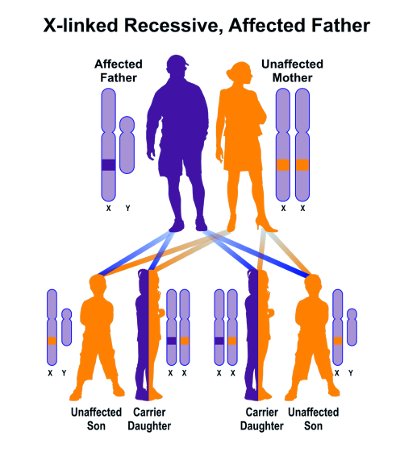
- Famiglia. La sindrome di Hunter è causata da un cromosoma difettoso, e un bambino deve ereditare il cromosoma difettoso per sviluppare la malattia. La sindrome di Hunter è una patologia X-linked recessiva.
- Sesso. La sindrome di Hunter quasi sempre si verifica nei maschi.
Complicazioni
Una varietà di complicazioni possono verificarsi con la sindrome di Hunter a seconda del tipo e gravità della malattia. Queste possono includere:
- Complicazioni respiratorie. Tutte le forme di MPS, tra cui la sindrome di Hunter, comportano complicazioni respiratorie che contribuiscono alla disabilità del bambino e a volte causano il decesso. Una lingua allargata, gengive ispessite,ispessimento delle cavità nasali e della trachea (trachea) rendono difficile la respirazione.
- Complicazioni cardiache. L’indurimento del tessuto associato con la sindrome di Hunter può causare progressivo ispessimento delle valvole del cuore. Ciò causa la chiusura impropria di valvole cardiache. Come risultato, il cuore e altre parti del corpo non ricevono sangue in modo efficiente.
L’ispessimento del tessuto può anche causare restringimento dell’aorta (coartazione) e di altri vasi sanguigni. Questo a sua volta può portare a pressione alta (ipertensione) e il restringimento delle arterie nei polmoni (ipertensione polmonare).
- Complicanze del tessuto scheletrico e connettivo. Lo stoccaggio dei glicosaminoglicani in tessuti connettivi riduce la crescita del bambino, provocando dolore e malformazioni anatomiche.
Quasi tutti i pazienti affetti dalla sindrome di Hunter sperimentano rigidità articolare. La rigidità è causata da gonfiore dei tessuti connettivi comuni e anomalie di cartilagine e ossa. Se il bambino ha dolore, è ovviamente portato a muoversi di meno.
Il gruppo di anomalie tipicamente visto nelle ossa delle persone con sindrome di Hunter si chiama disostosi multipla. I bambini con queste alterazioni possono sviluppare cifoscoliosi, anomalie delle coste, braccia, dita, gambe e pelvi.
- Ernie (inguinale e ombelicale) sono comuni nella sindrome di Hunter. Si verificano a causa di problemi con il tessuto connettivo. L’ernia si verifica quando i tessuti molli, di solito parte dell’intestino, sporgono attraverso un punto debole o lacerazione nella parete addominale inferiore. Le ernie associate con la sindrome di Hunter possono diventare molto grandi e sono spesso uno dei primi segni della malattia. L’allargamento del fegato e milza (epatosplenomegalia), può aumentare la pressione nell’addome, provocando un ernia.
- Complicazioni del cervello e sistema nervoso. Una serie di complicazioni neurologiche possono essere presenti e continuare a svilupparsi nei bambini con sindrome di Hunter. Molti problemi neurologici sono causati da un accumulo di liquidi in eccesso nel cervello idrocefalo). La pressione da questi fluidi può causare problemi al midollo spinale e può influenzare gli occhi così come altri organi sensoriali, causando forti mal di testa, che interferiscono con la visione e modificano lo stato mentale del bambino.
Il bambino può anche sviluppare una condizione in cui le membrane che circondano il midollo spinale possono diventare spesse (ipertrofica pachimeningite cervicale). Ciò causa compressione del midollo spinale superiore.
- Altri disturbi, come la sindrome del tunnel carpale, possono derivare da compressione del nervo che accade a causa di deformità ossee e glicosaminoglicani nei tessuti.
- Comportamento anomalo. Spesso alcuni bambini sono iperattivi e hanno difficoltà a prestare attenzione. Il bambino può anche comportarsi in modo aggressivo e sembrare incapace di percepire pericolo. Con il tempo, questi problemi di comportamento tendono a diventare meno gravi.
- Possono anche verificarsi convulsioni nei bambini affeti da sindrome di Hunter.
- Recupero più lento dalle malattie. I tempi di recupero da malattie infantili normali possono essere più lunghi per i bambini con sindrome di Hunter o altre sindromi MPS.
Diagnosi
I bambini nati con la sindrome di Hunter appaiono quasi sempre sani alla nascita. Il cambio nelle caratteristiche facciali sono spesso il primo segno evidente che qualcosa non va.
Per confermare la diagnosi di sindrome di Hunter, il medico effettuerà degli esami del sangue, delle urine o dei tessuti alla ricerca di glicosaminoglicani in eccesso nelle urine o una carenza di enzimi nei fluidi del corpo o nelle cellule. Inoltre, l’analisi genetica può confermare la diagnosi.
A volte un altro problema di salute può portare ad una diagnosi di sindrome di Hunter. Per esempio, se il bambino ha la polmonite ricorrente, una radiografia del torace può mostrare vertebre e coste di forma irregolare, un segno comune di questa sindrome. Tuttavia, poiché la malattia progredisce lentamente e suoi segni e sintomi si sovrappongono con altri disturbi, una diagnosi definitiva può richiedere molto tempo.
Diagnosi prenatale
La diagnosi prenatale del liquido che circonda il bambino (amniocentesi) o di un campione di tessuto dalla placenta (villi coriali) può verificare se il nascituro porta una copia del gene difettoso o è affetto da questo disturbo.
Trattamenti e cure
Poiché non esiste alcuna cura per la sindrome di Hunter, il trattamento si concentra sulla gestione di segni, sintomi e complicanz, per fornire un certo sollievo al bambino.
Anche se non esiste alcuna cura per la sindrome di Hunter o per altre sindromi MPS, alcuni trattamenti hanno avuto un certo successo rallentando il progresso della malattia e diminuendone la gravità.
Questi trattamenti emergenti comprendono:
- Il trapianto di midollo osseo. Il trapianto di midollo osseo può essere usato per trattare alcuni sintomi in forme più lievi della sindrome di Hunter. Il midollo osseo è preso dal fianco del donatore e trapiantato al bambino, iniettandolo in vena. Questo trattamento può contribuire ad alleviare i problemi di respirazione, di mobilità e funzione del cuore, fegato e milza.
- Terapia enzimatica. Questo trattamento utilizza enzimi artificiali o genetici, che vengono iniettaie direttamente nel sangue del bambino, per sostituire gli enzimi mancanti o difettosi. Questo trattamento è ancora in fase di studio.
- La terapia genica. La sostituzione del cromosoma responsabile della produzione dell’enzima mancante potrebbe teoricamente curare la sindrome di Hunter, ma la ricerca non è ancora a buon punto.
Trattamenti per le complicanze
- Sollievo dalla complicanze respiratorie. La rimozione delle tonsille e delle adenoidi può aprire le vie aeree del bambino e alleviare l’apnea del sonno. Ma, come la malattia progredisce, i tessuti continuano ad addensarsi e questi problemi possono tornare. Apparecchi di respirazione che utilizzano la pressione dell’aria per mantenere la pervietà delle vie aeree possno aiutare con le ostruzioni delle vie aeree superiori e l’apnea del sonno. Mantenere vie aeree del bambino pervie può evitare bassi livelli di ossigeno nel sangue (ipossiemia).
- Affrontare complicazioni cardiache. Il medico del bambino vorrà guardare da vicino le complicanze cardiovascolari, come ipertensione, soffio al cuore e problemi alle valvole cardiache. Se il bambino ha gravi problemi cardiovascolari, il medico può raccomandare un intervento chirurgico per sostituire le valvole cardiache.
- Il trattamento per problemi scheletrici e del tessuto connettivo. La flessibilità delle articolazioni del bambino può essere migliorata con la terapia fisica, che aiuta a mantenere la funzione articolare. Tuttavia, la terapia fisica non può fermare il progressivo declino del movimento articolare.
- La chirurgia è in grado di riparare le ernie, ma a causa della debolezza nei tessuti connettivi, i risultati di solito non sono perfetti. La procedura ha spesso bisogno di essere ripetuta.
- Gestione delle complicanze neurologiche. Problemi associati con l’accumulo di fluido intorno al cervello e midollo spinale sono difficili da affrontare a causa dei rischi insiti nel trattamento di queste parti del corpo. Il pediatra può raccomandare un intervento chirurgico per drenare i liquidi in eccesso o rimuovere l’eccesso di tessuti. Se il bambino ha crisi epilettiche, il medico può prescrivere farmaci anticonvulsivanti.
- Gestione dei problemi comportamentali. Se il bambino sviluppa comportamenti anomali come conseguenza della sindrome di Hunter, un ambiente sicuro in casa è uno dei modi più importanti per gestire questa sfida. Trattare i problemi di comportamento con i farmaci ha un successo limitato, poiché la maggior parte dei farmaci hanno effetti collaterali che possono dare altre complicazioni della malattia.
- Affrontare i problemi del sonno. I farmaci compresi sedativi e, soprattutto la melatonina possono migliorare il sonno.
Martin R, et al. Il riconoscimento e la diagnosi di mucopolisaccaridosi II (sindrome di Hunter). Pediatrics. 2008; 121: e377.
MPS II (sindrome di Hunter). Nazionale MPS Society. http://www.mpssociety.org/index.php?option=com_content&view=article&id=129&Itemid=18. Consultato il 6 maggio 2010.
Mucopolisaccaridosi scheda. Istituto nazionale dei disordini neurologici e ictus. http://www.ninds.nih.gov/disorders/mucopolysaccharidoses/detail_mucopolysaccharidoses.htm. Accesso effettuato nel maggio 8, 2010.
Kakkis E, et al. Caratteristiche cliniche e diagnosi delle mucopolisaccaridosi. http://www.uptodate.com/home/index.html. Consultato il 5 maggio 2010.
Kakkis E, et al. Complicanze e gestione delle mucopolisaccaridosi. http://www.uptodate.com/home/index.html. Consultato il 5 maggio 2010.
Münzer J, et al. Gestione multidisciplinare della sindrome di Hunter. Pediatrics. 2009; 124: e1228.
Newborn screening. Centers for Disease Control and Prevention. http://www.cdc.gov/nbslabbulletin/bulletin.html~~V. Consultato il 6 maggio 2010.
Guffon N, et al. Trapianto di midollo osseo in bambini affetti da sindrome di Hunter: Esito dopo 7 ai 17 anni. Journal of Pediatrics. 2009; 154:733.
Elaprase (prescrizione informazioni). Cambridge, Mass.: Shire terapie genetiche umane; 2007. http://www.elaprase.com/pdf/ElaprasePI40-0120_REV_0_GT4.pdf. Consultato il 5 maggio 2010.
La sicurezza e gli esiti clinici nei pazienti con sindrome di Hunter 5 anni di età e più giovani terapia idursulfasi ricezione. ClinicalTrials.gov. http://clinicaltrials.gov/ct2/show/NCT00607386. Consultato il 6 maggio 2010.
Burrow TA, et al. Revisione dell’utilizzo di idursulfasi nel trattamento di mucopolisaccaridosi II. Biologics: Targets & terapia. 2008; 2:311.
Friso A, et al. Genisteina riduce i livelli di glicosaminoglicani in un modello murino di mucopolisaccaridosi di tipo II. British Journal of Pharmacology. 2010; 159:1082.
Piotrowska E, et al. Genisteina-mediata inibizione della sintesi glicosamminoglicano come base per l’espressione del gene-terapia mirata isoflavone per mucopolisaccaridosi. European Journal of Human Genetics. 2006; 14:846.